溶瘤病毒是指将天然的或经过基因重组的病毒选择性地感染癌细胞,通过病毒自身的功能杀死并裂解癌细胞。这时,若再加以一定的免疫刺激,破裂的癌细胞能够引起系统性的免疫反应,引导免疫系统对其它癌细胞展开攻击。美国FDA已经批准了talimogene laherparepvec (T-VEC)用于治疗黑色素瘤,它是一种基于单纯疱疹病毒的溶瘤病毒疗法。
免疫检查点抑制剂正在广为人所知,CTLA-4和PD-1/PD-L1抑制剂都是通过阻断癌细胞抑制机体免疫功能的信号通路,来激活免疫系统对癌细胞展开攻击。不过,目前获批的PD-1/PD-L1抑制剂只能针对表达一定程度PD-L1的肿瘤,而对于那些不表达或者表达较少PD-L1的“冷”肿瘤无能为力。
来自匹兹堡大学的科研人员在这次的研究中发现,当他们使用牛痘病毒感染癌细胞后,被病毒激活的免疫系统使得更多的T细胞进入了肿瘤组织。面对T细胞的侵入,癌细胞会产生自我保护机制来逃过免疫攻击,其中一种主要办法就是增加PD-L1的表达。科研人员敏锐地意识到,通过这个方法可以将那些原本对PD-1/PD-L1抑制剂不敏感的“冷”肿瘤,变为敏感的“热”肿瘤。这时再加入PD-1/PD-L1抑制剂就有可能取得叠加的效果。
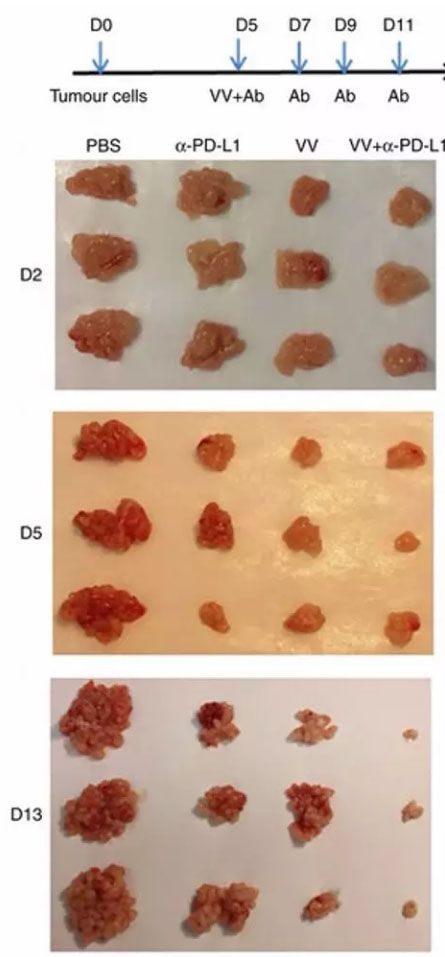
T-VEC和PD-L1抗体对小鼠肿瘤的联合抑制(图片来源:《Nature Communications》)
在一个小鼠结肠癌模型中进行的实验证实了这一点,单独使用溶瘤病毒或者PD-L1单抗一周之后,肿瘤的大小减小了一半左右,而两者联用,能够减小肿瘤80%以上,其中超过40%的小鼠体内肿瘤完全消失。并且两者联用能够延长患癌小鼠的平均生存时间超过一个月。进一步的研究发现,两种疗法联用显着地增加了肿瘤特异的CD4和CD8阳性的T细胞数量,并产生了系统性的针对肿瘤的免疫反应。
这项令人激动的研究展示出了联合溶瘤病毒和免疫检查点抑制剂这两种疗法的强大威力。通过使用溶瘤病毒,大大增加了对免疫检查点抑制剂敏感的肿瘤类型和数量。我们希望在不久的将来就能看到这种组合进入临床应用,造福更多的癌症患者。